- Startseite Mikrochemie
- Geschichte und Forscher
- Nichtquant. Techniken
- Quantitative Techniken
- Mikrochemie des Metallurgical Project (Manh.Proj)
- Die Mikrowaagen des "Metallurgical Project"
- Anwendungsbeispiele der Mikrochemie
- -unbekanntes Mineral
- -Erfassungsgrenze für Fe(III)
- -Neusilber-Analyse
- -Mixit-Analyse
- -Mikrocolorimetrie
- Mikrodichtebestimmung
- -Hg-Nachweis in Zinnober
- -Goldnachweis in Coloradorit
- -Untersuchung von Kolwezit
- Ultramikro-Nachweise auf "condenser rod"
- Mikrochemische Komplexometrie (Bi neben Pb)
- Mikro-Iodometrie von Cobalt in Gemischen
- Mikrochem. Unters. an einem Mineral
QUANTITATIVE (ULTRA-) MIKROCHEMIE
Mikro-Elektrogravimetrie
Die Nutzbarmachung der Elektrogravimetrie für die Mikrochemie ist hauptsächlich den Mikrochemikern Pregl, Emich und Donau (siehe "Geschichte und Forscher") zu verdanken.
Die unten sichtbare Anordnung entspricht am ehesten der von J.Donau, die er 1939 in der Zeitschrift "Mikrochemie" vorgestellt hat.
Ein kleines Platinblech wird zurechtgeschnitten, um gerade die notwendige Flüssigkeitsmenge aufnehmen zu können. Die Blechdicke sollte gerade noch ermöglichen, eine dauerhafte Vertiefung darin zu schaffen. Ein möglichst geringes Gewicht erlaubt später einen empfindlicheren Messbereich an der CAHN-Waage.

Das Blech wird zur Kathode. Ein adäquater Platinstab wird zur Anode. Der Einsatz geeigneter Mikromanipulatoren erlaubt die Variation der Eintauchtiefe in unterschiedliche Tropfenformen.


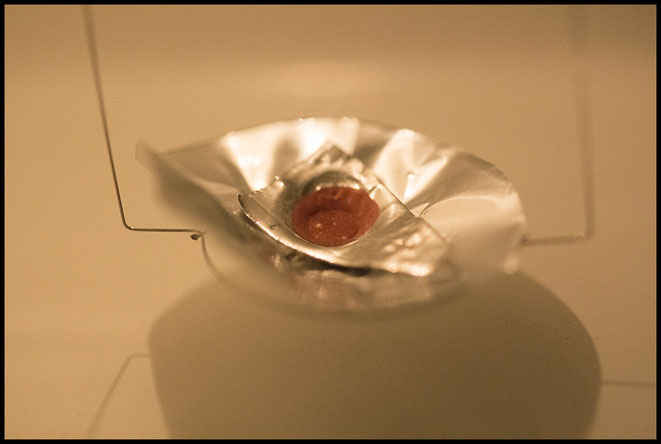
Hier sind 20 µl einer Kupfersulfatlösung aufgebracht. Eine Spannung von etwa 2,4 Volt wird angelegt. Schon nach wenigen Sekunden zeigt sich (siehe Bild) eine "Rosa"-färbung der Pt-Kathode als Zeichen der beginnenden Cu-Abscheidung. Wenige, kleine Gasbläschen treten auf; eine Durchmischung wird allein hierdurch gewährleistet.

seitliche Perspektive zur Erkennung der Eintauchtiefe.

Oben das Bild nach etwa 10 Minuten.
Das gesamte Kupfer ist auf der Platinkathode abgeschieden.
Noch unter Spannung wird die verbliebene Flüssigkeit mit einer Kapillarpipette abgezogen, die Kathode schließlich mit aqua dest gespült und für 30 min bei 110°C getrocknet.
Die getrocknete "Kathode" mit dem Cu-Niederschlag wird nun mithilfe einer CAHN-Mikrowaage (CAHN Gram Electrobalance, Paramount/California)) mit einer Empfindlichkeit von bis zu 0,1 µg (!) gewogen.
Die Reproduzierbarkeit der Ergebnisse zeigt eine gute Transformation der Methode der Elektrogravimetrie in die Mikrochemie an.

Die "CAHN"- Mikrowaage beruht auf dem Prinzip der Torsion einer Spule in einem Magneten und der elektromagnetischen Messung der Rückstellkräfte.
Bis zu einem Wägebereich von 5 mg erlaubt sie eine Messempfindlichkeit von 0,1 µg (100 ng); diese verringert sich in höheren Messbereichen.
Die Waagen wurden seit den späten 50er Jahren hergestellt und in immer besseren Ausführungen über Jahrzehnte gebaut.
Sie ist sehr robust und weitgehend unempfindlich gegen Erschütterungen, Luftströhmungen und Temperaturschwankungen.
Gute Exemplare sind kaum noch zu bekommen (wenn, dann auf dem amerikanischen Markt)

Die Empfindlichkeit der Methode ist hoch. Im Bild oben sind etwa 500 ng (0,5 µg) Cu in einem 5 mm Platintiegel deponiert. Nachweise von Kupfermengen im zweistelligen Nanogramm-Bereich sind so rein optisch möglich.
Mengen oft noch deutlich darunter, auch nichtfarbiger Metalle, lassen sich leicht mit mikrochemischen Nachweisen (z.B. Kristallformen oder Farbreaktionen) identifizieren.
Unter geeigneten Bedingungen (z.B. basische oder gepufferte Lösungen) lassen sich auch Metalle wie Zink (Bild unten), Nickel oder Cobalt elektrolytisch abscheiden.

